
El óxido hipocloroso, llamado también Ácido hipocloroso o Clorato de hidrógeno, es la denominación que se le otorga al ácido que resulta de la unión del óxido ácido de cloro con H2O.
Por otra parte, es importante indicar, que recibe ese nombre debido a que el cloro actúa con el estado de oxidación +1, que es el menor de los cuatro positivos que posee:
+1, +3, +5 y +7.
Propiedades físicas
- Masa molar 52.46 g/mol
Propiedades químicas
- Acidez: 7.49 pKa
- Solubilidad en agua: Soluble
- Peligrosidad
Fórmula química y modo de obtención
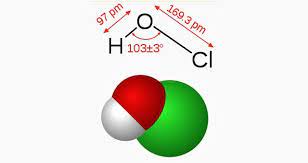
Es importante destacar, que la fórmula química del óxido hipocloroso es:
HClO
Esta se obtiene mediante:
- Formación del óxido ácido:
- Formulación: Cl2+O2 → Cl+1 O-2
Cruce de valencias o estado de oxidación:
- Cl2+O2 → Cl+12 O-21
Por otra parte, el 1 que tiene el oxígeno no es necesario escribirlo, dando como resultado:
- Cl2O.
- Formación del ácido:
- Formulación: Cl2O + H2O →
Formación del ácido: Cl2O + H2O → H2Cl2O2
Como la atomicidad es igual se simplifica (H2Cl2O2) y se obtiene por resultado:
HClO
A la luz de lo anterior, podemos afirmar que químicamente el HClO puede ser obtenido por diferentes métodos.
Obtención química del HClO:
- Hidrólisis de gas de cloro (Cl2 + H2O → HClO + H+ + Cl-)
- Electrólisis de solución de sal (2Cl → Cl2 + 2e-) y (Cl2 + H2O → HClO + H+ +Cl-)
- Acidificación de hipoclorito (OCl- + H+ → HClO)
Características del óxido hipocloroso
Es posible afirmar que el óxido hipocloroso puede describirse químicamente como:
- Un ion no disociado del cloro.
- Dependiente del oxígeno.
- Altamente inestable.
- Y, también altamente reactivo.
Además, es uno de los ácidos hipohalogenados más fuertes.
Por ello, es también uno de los más poderosos oxidantes entre los oxácidos clorados.
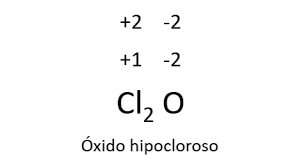
Y, también es el responsable directo de la acción bactericida de los compuestos derivados del cloro
El ácido hipocloroso o desinfectante
El ácido hipocloroso forma parte de un nuevo grupo de sustancias microbicidas conocidas como «moléculas antimicrobianas no antibióticas», o, desinfectantes
Al respecto podemos decir que, estas sustancias actúan por oxidación de la materia orgánica.
Se puede afirmar que biológicamente, se ha encontrado en el cuerpo humano en muy bajas concentraciones
Por otra parte, el óxido o ácido hipocloroso está clasificado dentro de un grupo de pequeñas moléculas conocidas como especies reactivas del oxígeno (ROS).
- Sintetizadas por neutrófilos y macrófagos células del sistema inmune durante un proceso inmunológico conocido como «estallido respiratorio».
- Este proceso se da durante la fagocitosis de antígenos en reacción con la enzima mieloperoxidasa peróxido de hidrógeno (H2O2) y un ion de cloro.
Del mismo modo funciona como una sustancia quimiotáctica que permite un excelente control microbiano y activación del sistema de defensa que facilita la rápida e inocua reparación de tejidos.
La técnica Carrel-Dakin
Se puede afirmar, que los usos terapéuticos del HClO se inician durante la Primera Guerra Mundial, cuando se incrementó las muertes por infecciones en los soldados.
Esta situación llevó a médicos y científicos a iniciar la búsqueda de:
- Por una parte, de una sustancia desinfectante.
- La que se aplicara directamente en las heridas.
- Con la capacidad de destruir microorganismos y sus toxinas.
- Y, que no dañara el tejido normal.
En 1915, los investigadores Alexis Carrel y Henry Dakin obtuvieron una solución de hipoclorito de sodio tamponado, llamada solución de Dakin, el cual generaba concentraciones ideales de HClO.
De esta manera:
- Trataron heridas.
- Fracturas.
- Articulaciones supurativas.
- Y, demás patologías.
- Para ello, utilizaron entre 1 a 2 litros/día de la solución tamponada.
Tanto este procedimiento, como el nombre de la solución, son conocidos como la técnica de Carrel‐Dakin, el que fue usado durante la Guerra para tratar las heridas infectadas.
No obstante el método perdiera vigencia por:
- La baja estabilidad de la solución.
- El dispendioso método de preparación.
- Y, los grandes volúmenes requeridos.
Posteriormente, en 1980 se retoman las investigaciones sobre el ácido hipocloroso.
En 1989 el científico británico J. Weiss observa in vitro el poder bactericida del HClO liberado por neutrófilos.
De la misma forma, laboratorios a nivel mundial buscan soluciones estables de HClO con fines terapéuticos, dirigidas al tratamiento de diversas patologías de piel.
En este sentido, en 1993, el investigador colombiano Justo Calderón, logra estabilizar la molécula de HClO con fines médicos para el tratamiento y control de infecciones en heridas crónicas y complejas por ejemplo:
- Úlceras de miembros inferiores: úlceras varicosas, isquémicas, úlceras de pie diabético.
- Quemaduras de segundo y tercer grado.
- También, infecciones cutáneas.
- Heridas limpias, contaminadas y/o con tejido necrótico.
- Celulitis, abscesos, hongos tópicos.
El óxido hipocloroso, otros usos
Por otra parte, veamos algunos otros usos del HCIO:
- Esta sustancia en concentraciones elevadas trabaja muy bien como desinfectante de superficies.
- También se usa como sustancia dirigida a la inactivación de desechos hospitalarios.
Es posible afirmar, que el HCIO está permitido para:
- La piel,
- También en superficies.
- El ámbito sanitario.
- El área veterinaria.
- La industria agroalimentaria.
- Y, además, para la desinfección del agua.
- Finalmente, por sus propiedades antiseborreico, oxidante, antimicrobiano y desodorante, puede ser utilizado para fabricar productos cosméticos.
