
Los hidrácidos son una combinación binaria de hidrógeno y un elemento no metálico, y son también llamados hidruros no metálicos, se les conoce también como ácido hidrácido.
Es importante señalar, que los hidrácidos componen una familia de compuestos binarios de gran interés para la industria química.
En cuanto a su fórmula química general, esta puede expresarse como:
- HX
Donde, H corresponde al átomo de hidrógeno
Y, la X representa:
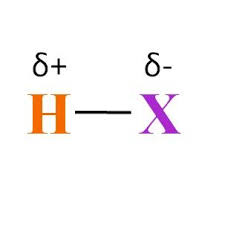
- un símbolo del elemento no metálico, sea este de la familia de los halógenos: cloro, bromo, yodo y flúor.
H + F, Cl, Br, T = grupo 17
- O, un elemento del grupo de los calcógenos como el azufre, selenio o teluro.
H + S, Se, Te = grupo 16
Por otra parte, al momento de formular, se coloca primero más electropositivo y a continuación el más electronegativo. Por tanto, primero el hidrógeno y después los otros.
Además,
- el grupo 17 presenta una valencia – 1
- y el grupo 16 presenta una valencia – 2.
Características físicas de los hidrácidos
En lo que respecta a las características físicas de los hidrácidos tenemos que:
En primer lugar, son solubles en agua.
- Estas sustancias son muy solubles en agua y originan soluciones transparentes o amarillentas dependiendo de la concentración de la solución.
También desprenden vapores densos.
- En este sentido, la emanación de vapores tiene relación a la facilidad con la que reaccionan con el vapor de agua en el ambiente.
Y, por último, sus soluciones conducen la electricidad.
- A pesar de ser compuestos gaseosos, forman soluciones electrolíticas al disolverse en agua.
- Liberando iones que permiten el paso de la corriente eléctrica.
Características químicas de los hidrácidos
Es importante destacar, que entre sus características químicas los hidrácidos, por una parte:
Forman soluciones muy ácidas.
- Es decir, los hidrácidos tienen gran facilidad para donar protones en forma de iones hidronio.
- Lo que produce una reacción de equilibrio, es decir, si la reacción es termodinámicamente favorecida hacia la derecha, el HX liberará su protón, el cual será aceptado por el agua para dar el H3O+.
Fortaleza de los hidrácidos.
- Dependiendo de elemento no metálico al cual se encuentre unido el hidrógeno, el hidrácido será fuerte o débil.
Nomenclatura
En lo que respecta a la nomenclatura, es importante destacar que:
En sus formas anhidras y gaseosos, se nombran añadiendo la terminación “uro” al no metal, seguido de la palabra hidrógeno.
- Por ejemplo. El HCl, es un haluro formado por cloro e hidrógeno, por lo que se nombra como cloruro de hidrógeno.
Al contrario, cuando el haluro se encuentra en disolución acuosa, se obtiene como tal el hidrácido. Y se nombra añadiendo el sufijo hídrico y se antepone la palabra ácido;
- Como ejemplo: el HCl(ac) se nombra como ácido clorhídrico.
Ejemplos de hidrácidos
A pesar de ser muy limitadas las combinaciones naturales de estos compuestos, podemos señalar, entre otros:
El Ácido sulfhídrico (H2S):
En primer lugar es la solución acuosa del sulfuro de hidrógeno,
- Además, es altamente tóxico
- y presenta un fuerte olor huevo podrido.
- Por otra parte, es un hidrácido poliatómico, porque contiene más de dos átomos.
- Se considera un elemento binario porque está compuesto solo de dos elementos, S y H.
El Ácido clorhídrico (HCl):
Respecto a este elemento podemos decir que es uno de los más conocidos.
- Es utilizado en productos de limpieza
- y forma parte de la composición de los jugos gástricos.
- Además, se caracteriza por un fuerte olor y sabor agrio.
Por otra parte, está el Ácido fluorhídrico (HF):
Es importante destacar, que este hidrácido forma fuertes puentes de hidrógeno, a tal punto que en agua es un ácido débil.
- Es uno de los ácidos más peligrosos y corrosivos,
- conocido por atacar el vidrio.
- Sus soluciones son incoloras y con densidad similar al agua,
- tiene un olor agudo y penetrante.
También está el Ácido Bromhídrico (HBr):
Debemos mencionar, que este es producto de la solución acuosa del bromuro de hidrógeno, por lo que:
- Es un ácido muy fuerte.
- Y, además muy volátil.
Además, el Ácido selenhídrico:
En lo que respecta a este elemento podemos decir que:
- Es la disolución del seleniuro de hidrógeno.
- Presenta un olor irritante.
- Y, es sumamente venenoso.
Tenemos también, el Ácido yodhídrico (HY):
Este ácido es el resultante de la disolución del yoduro de hidrógeno.
- Posee la peculiaridad de ser irritante y corrosivo.
Por último, el Ácido telurhídrico:
Hay que tomar en cuenta que el telurio tiene cierto carácter metálico, sin embargo:
- La solución del telurio de hidrógeno es muy venenosa.
- Y altamente condensable.
Usos más comunes
Uno de los componentes de los productos limpiadores, es justamente los hidrácidos.
Por cuanto, sus protones ácidos se asocian con los compuestos de las impurezas:
- Actúan haciéndolos más solubles.
- Y, haciendo posible que se desprendan fácilmente de las superficies.
- Al respecto, por ejemplo el ácido clorhídrico es un buen removedor de manchas de baldosas y piezas sanitarias.
Además, son utilizados como catalizadores ácidos en diversas reacciones, por ejemplo:
En la industria petrolera se emplean los hidrácidos en diversos procesos de refinación.
Por otra parte, también son muy utilizados para la síntesis de haluros de compuestos orgánicos específicos.
